Diarrea viral bovina: necesidad de erradicación y cómo lograrla
Resumen
El año 2016 vio el lanzamiento de BVDFree England: un esquema voluntario liderado por la industria que trabaja para eliminar la diarrea viral bovina (BVD) de todo el ganado en Inglaterra para 2022. En junio de 2018, se lanzó la iniciativa BVD Stamp It Out, inyectando £ 5.7 millones en erradicación en Inglaterra. Mediante el uso del Programa de Desarrollo Rural para la financiación de Inglaterra, asegurado hasta finales de 2020, su objetivo es involucrar al 50% del rebaño de cría trabajando con prácticas veterinarias locales que buscan ofrecer esta financiación a los clientes. BVD es citada como la tercera enfermedad económicamente más devastadora en la industria láctea después de la mastitis y la cojera. Se cree que le cuesta a la industria ganadera en el Reino Unido hasta £ 61 millones al año. La agricultura del Reino Unido enfrenta una presión creciente del consumidor para mejorar la eficiencia, reducir el uso de medicamentos y mejorar aún más el bienestar animal. Una enfermedad que afecta mucho más que el animal infectado persistentemente, al eliminar la BVD del rebaño del Reino Unido, podemos avanzar mucho en la mejora de la fertilidad, la productividad y la salud y el bienestar de las vacas, tanto en el sector lácteo como en el de la carne.
 Un pestivirus de alta variabilidad genética (otros incluyen la peste porcina clásica y la enfermedad fronteriza de las ovejas), los primeros informes (1953) de diarrea viral bovina (BVD) fueron de una diarrea aguda altamente infecciosa donde la mayoría de los animales se recuperaron rápidamente, aunque del 4% al 8 El% murió de enfermedad de la mucosa.
Un pestivirus de alta variabilidad genética (otros incluyen la peste porcina clásica y la enfermedad fronteriza de las ovejas), los primeros informes (1953) de diarrea viral bovina (BVD) fueron de una diarrea aguda altamente infecciosa donde la mayoría de los animales se recuperaron rápidamente, aunque del 4% al 8 El% murió de enfermedad de la mucosa.
En estos días, los practicantes generalmente aceptarían la diarrea como una presentación menos común, con problemas de fertilidad y salud de las pantorrillas que a menudo señalan preguntas sobre el estado de BVD de un rebaño. Ya en 1956, se descubrió que los abortos eran un hallazgo constante en rebaños con brotes de enfermedades, con infección transplacentaria demostrada en la década de 1970. Estas presentaciones de enfermedades son las que conducen a una interrupción económica masiva en una granja, a una pobre fertilidad y producción en vacas y a una función inmune debilitada en la pantorrilla.
Los animales no preñados que se encuentran con la enfermedad no sufrirán una enfermedad clínica marcada. Lo que puede presentar son pirexia, leucopenia de los días 3 a 7 y recuperación limitada del virus de las secreciones nasales durante los primeros 3 a 10 días. Los efectos inmunosupresores los hacen más susceptibles a otras infecciones, como la neumonía y la enfermedad entérica, y se han establecido vínculos para aumentar la incidencia de TB en el rebaño afectado por BVD.
En la vaca adulta, puede ver caída de la leche o restregar y pérdidas reproductivas. En la pantorrilla con infecciones duales (BVD más neumonía / diarrea), es probable que exista una morbilidad y mortalidad más significativas. Sin embargo, no se puede subestimar la importancia de estas infecciones transitorias, ya que son responsables del 93% de todas las infecciones en el útero que resultan en el nacimiento de terneros con infección persistente (IP).
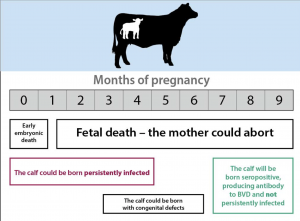
La infección en el útero de la pantorrilla conduce a resultados bastante diferentes, descritos en detalle en otra parte (Figura 1). La infección temprana puede provocar aborto, reabsorción fetal o muerte fetal. Una infección muy tardía (seis meses más de gestación) puede provocar una pantorrilla normal. Las terneras infectadas a mediados del embarazo pueden desarrollar defectos congénitos de deformidades neurológicas o de extremidades.
El subconjunto crucialmente importante de terneros se infecta antes de que se desarrolle la inmunocompetencia (aproximadamente 120 días), pero sobrevive hasta el nacimiento y puede llegar a la edad adulta. Se ha demostrado que son inmunotolerantes al virus, que no producen anticuerpos y que efectivamente son terneros PI. Son estos terneros los que podrían desarrollar enfermedad de la mucosa y son fundamentales en la propagación y control de la enfermedad (Figuras 2a y 2b).

Figura 2a. Vista clásica de un ternero infectado persistentemente (PI) pobremente prosperado. Imagen: Servicio Nacional de Información sobre Enfermedades Animales.
El mantenimiento y la propagación en un rebaño es por el animal PI, que actúa efectivamente como un súper eliminador, excretando 1,000 veces más virus en las secreciones corporales en comparación con un animal infectado de forma transitoria. Los experimentos muestran que la supervivencia ambiental del virus BVD (BVDV) depende de los niveles de temperatura y humedad, con una supervivencia máxima en la lechada de granja bovina a 5 ° C durante tres semanas y a 20 ° C durante tres días.
Existen informes anecdóticos y experimentales de transmisión indirecta de BVDV desde corrales contaminados, guantes de examen rectal, agujas hipodérmicas, pinzas nasales y aire ambiente. Se ha encontrado que un tubo de sangre PI diluido con 700L de agua sigue siendo infeccioso1-3. Dos especies distintas de BVDV pertenecen principalmente a la distribución geográfica del virus. BVDV-1a a BVDV-1n tienen una distribución mundial, con la mayoría de los aislamientos encontrados en el Reino Unido que pertenecen al grupo BVDV-1a. Los virus BVDV2 estaban históricamente restringidos a EE. UU. Y Canadá, aunque se sabía que estaba activo en el Reino Unido en 2007.
Estudios más recientes no han podido identificarlo circulando activamente en el Reino Unido. Sin embargo, con los movimientos internacionales de ganado, sigue siendo un riesgo significativo para la población de ganado del Reino Unido4.

Además de esto, existen dos biotipos distintos para cada especie de BVDV: el no citopático, que persiste en la población bovina (en forma de animales PI), y el biotipo citopático, que surge después de una variedad de eventos de mutación o recombinación con otras cepas de BVDV que pueden causar enfermedad de la mucosa en el animal PI.
¿Por qué es necesaria la erradicación?
La BVD se considera generalizada en el Reino Unido, ya que el 90% de los rebaños muestran cierta exposición al virus. Las estimaciones de la prevalencia de animales PI dentro de esos rebaños están entre 0.3% y 3%.
La BVD está muy extendida en América del Norte y algunos países de Europa central, mientras que otros países han lanzado esquemas de erradicación a gran escala desde 1993. Las Islas Shetland, los países escandinavos, Alemania y Suiza han liderado el camino con la erradicación. A pesar de las diferencias en el apoyo legal y la prevalencia inicial (1% a 50%), estos países han entrado en fases finales de erradicación después de 10 años, con Suiza y los países escandinavos libres de BVD (Figura 3) 5,6.
Más localmente, Escocia, Irlanda e Irlanda del Norte ya han implementado programas obligatorios dirigidos por el gobierno con los cambios legislativos correspondientes que se centran en las pruebas obligatorias y las restricciones comerciales en granjas y / o animales que aún no se han probado. Escocia entró en la fase 5: Cumplimiento en 2019.
Esto se centró en proteger a todos los rebaños negativos a toda costa, con matrices integrales de cumplimiento de incumplimiento seguidas por las autoridades locales.
Irlanda comenzó las pruebas obligatorias en 2013, notificando a los vecinos y las restricciones de movimiento en la identificación de los animales PI, hasta que se eliminaron. Gales tiene un programa voluntario liderado por la industria que se lanzó en julio de 2017.
Las granjas que dieron positivo luego recibieron fondos del Programa de Desarrollo Rural del Gobierno de Gales para ayudar a la identificación de los animales PI. A partir de noviembre de 2019, el 75% en el país había sido probado, mostrando que el 28% de los rebaños eran seropositivos y encontrando 243 animales
PI. En 2016, Inglaterra lanzó el esquema voluntario BVDFree England liderado por la industria (www.bvdfree.org.uk) pidiendo a los agricultores individuales que se registren en una base de datos nacional donde los estados de BVD son fácilmente accesibles. El plan tiene como objetivo facilitar la erradicación para 2022. En 2019, el 31 de diciembre se registraron 5.656 explotaciones, es decir, el 34,53% del total de ganado de cría inglés. En 2018, se lanzó el esquema BVD Stamp It Out utilizando un programa de desarrollo rural de £ 5.7 millones para financiamiento de Inglaterra. Esto busca involucrar al 50% del rebaño de cría del Reino Unido. A diciembre de 2019, 5.098 granjas están inscritas, con 4.200 de las que optan por inscribirse también en BVDFree England7.
Si Inglaterra no aborda la BVD, el impacto en las exportaciones sería inevitable. Debemos tratar de abordar la percepción de que nuestra falta de control sobre BVD, y otras enfermedades legales y no legales, nos deja una perspectiva de alto riesgo para el comercio de ganado (Panel 1).
Panel 1. ¿Por qué erradicar la BVD?
Mejora de la salud, el bienestar y la productividad de nuestros rebaños.
Reduzce las pérdidas financieras significativas debido a los rebaños positivos para el virus BVD (BVDV)
Elimina el riesgo de introducir BVDV a rebaños ingenuos Uso reducido de medicamentos – antibióticos
Progresa para mantenerse al día con los socios comerciales – siga operando
Reduce
los estresores psicológicos de los animales enfermos y la baja productividad del personal de la granja.
Cómo lograr la erradicación
BVD se encuentra en una muy buena posición para el veterinario entusiasta y el agricultor comprometido. Tenemos pruebas confiables y asequibles para la vigilancia de anticuerpos (exposición) y la búsqueda de antígenos (infección). También tenemos vacunas seguras y efectivas para reforzar la protección de un rebaño cuando nos enfrentamos a problemas de bioseguridad.
La erradicación a nivel de rebaño se puede lograr con el compromiso del agricultor y el veterinario por igual, en tan solo dos años. BVDFree England y el esquema BVD Stamp It Out se basan en principios comunes de control de enfermedades (Figuras 4a).
Paso 1: evaluar el rebaño Observe la bioseguridad, la vacunación, el historial de enfermedades (fertilidad, salud y producción del rebaño) y el riesgo de enfermedad en los últimos dos años. Planifica tu objetivo.
Paso 2: definir el estado del rebaño Muestra de animales: ya sea una prueba de verificación, un cribado de cría o una etiqueta y una prueba de todos los animales nacidos (para incluir nacidos muertos y abortos) durante dos años (Figura 4a).
Paso 3: plan de acción Identifique y descarte animales PI de una granja utilizando pruebas completas de todo el rebaño o pruebas estratégicas específicas. Por ejemplo, las muestras agrupadas de grupos de animales, las novillas de primera lactancia, el etiquetado y las pruebas de todas las terneras a pie, y la PCR de leche a granel pueden ayudar a reducir un grupo para pruebas individuales. Siempre revise las represas de cualquier resultado positivo. Todos los animales PI deben ser sacrificados del rebaño. Plan de control de bioseguridad y protección con vacunación según sea necesario.
Paso 4: Monitoreo y actualización Los exámenes repetidos de ganado joven cada 6 a 12 meses (observe los riesgos relativos) o el etiquetado y las pruebas de todas las crías nacidas durante dos años son pasos obligatorios para cumplir con BVDFree England o Cattle Health Certification Standards (CHeCS). El monitoreo trimestral de muestras de leche a granel de anticuerpos o antígenos puede ser útil, aunque puede requerir una interpretación reflexiva8.
Monitorear la bioseguridad y vacunar cuando sea necesario.
¿Qué pruebas se pueden hacer y cuándo?
Las pruebas ELISA de anticuerpos darán una idea de si el grupo de animales ha estado expuesto al BVDV. Esto se puede hacer como un cribado de cría de animales de 9 meses a 15 meses: de 5 a 10 de cada grupo de manejo de sangre individual (suero). Es importante que se evalúe a cada grupo de gestión, teniendo en cuenta el contacto nariz con nariz y el espacio aéreo compartido de al menos dos meses.
Para obtener más consejos sobre el muestreo grupal, visite https://bit.ly/2OrrX3Y La vigilancia de anticuerpos contra la leche a granel puede ser un complemento útil, pero no se reconoce su definición robusta del estado del rebaño y requiere una interpretación cuidadosa8.
Otra opción son las pruebas de antígeno: cuando una respuesta de anticuerpos muestra exposición, el objetivo es identificar la fuente de infección. La etiqueta y la prueba representan pruebas de antígeno PCR de tejido individuales asequibles y fáciles (los agricultores pueden hacerlo) (Figura 5). Las etiquetas pueden usarse como etiquetas de administración o para incluir números de identificación obligatorios. Cuando se usa como vigilancia total del rebaño, todos los terneros (incluidos los nacidos muertos) deben marcarse lo antes posible después del nacimiento para reducir la identificación de la infección transitoria circulatoria. Esto no se ve afectado por el anticuerpo derivado de la madre.
Una prueba de antígeno PCR de leche a granel (lo suficientemente sensible como para identificar 1 animal PI de 300 animales de ordeño) mostrará si el virus se secreta activamente en el tanque a granel. Es una prueba útil y económica, pero debe recordarse que solo ofrece una instantánea de las vacas que contribuyeron ese día. Además, pueden producirse falsos positivos con la vacuna viva modificada dentro de las cuatro semanas posteriores a la vacunación. Consulte a su laboratorio para obtener los números exactos de confianza.
Las pruebas de antígeno sanguíneo individuales disponibles incluyen PCR y ELISA de antígeno. Cualquier viremia individual en una primera muestra (mayor de 30 días de edad) debe, estrictamente hablando, volverse a analizar tres semanas después, ya que la viremia en un animal infectado de forma transitoria solo dura de 10 a 14 días. Las muestras posteriores que dan positivo confirman que el animal es PI.
No olvides los toros
Todos los toros PI producen semen infectado con BVDV. Además, la infección aguda (transitoria) del toro puede provocar una infección por BVDV de los tejidos testiculares y el semen, que, a su vez, a menudo es de baja calidad y, sin embargo, tiene el potencial de propagar BVDV a vaquillas seronegativas.
Además, en toros se ha demostrado que si bien pueden generar una respuesta inmune a los anticuerpos que producen infecciones transitorias, es posible que esos anticuerpos no siempre puedan cruzar la barrera de los testículos y, en un toro, el virus se eliminó continuamente en el inmunocompetente no virémico animal9.
Las técnicas normales de análisis de sangre habrían demostrado que este toro era inmune y no se había derramado, aunque habría representado un grave riesgo para las novillas ingenuas9.
Bioseguridad
La bioseguridad forma la base de cualquier plan de enfermedades infecciosas. Cada vez más, la industria busca a los agricultores para que se comprometan con esto de una manera más proactiva. Múltiples contratos de leche ahora buscan capacitación y revisiones anuales de bioseguridad con veterinarios.
Red Tractor Assurance está buscando granjas lecheras para tener un plan de erradicación de BVD en funcionamiento que abarque la bioseguridad. Además, una variedad de esquemas de acreditación (por ejemplo, CHeCS, Premium Cattle Health Scheme y HiHealth Herdcare) brindan un marco estructurado para que los rebaños de carne y lácteos reciban reconocimiento por su estricta bioseguridad.
En 2019, una encuesta de Inglaterra mostró que, del 62% de los rebaños que declararon que estaban cerrados, el 19% compró toros. La misma encuesta mostró que el 20% de aquellos que no sacrifican animales PI los venderán el 10. En particular, se ha producido una retención de animales PI superior a la prevista en los esquemas galeses e irlandeses, a pesar de no poder venderlos. Ahora los mataderos se han ofrecido para rechazar animales PI engordados para reducir las personas que intentan mantenerlos y terminarlos.
Los pasos recomendados para la bioseguridad en un plan de control de BVD son:
- Los límites de la granja deben ser seguros y evitar que el ganado se escape dentro o fuera de la granja.
- No hay contacto de nariz a nariz sobre las cercas: se recomienda una cerca doble con un espacio de al menos 3 m.
- Gestionar límites mediante el uso de campos límite para cultivos; pastar animales jóvenes o animales no preñados en campos de mayor riesgo si no pueden ser utilizados para cultivos.
- El ganado comprado se pondrá en cuarentena a menos que provenga de un rebaño del mismo estado de salud.
- Los animales en cuarentena deben mantenerse separados, incluido el espacio aéreo separado.
- Se prueban al comienzo y al final de un período de cuarentena apropiado (generalmente 28 días) antes de su liberación al rebaño.
- Los animales comprados durante el embarazo deben considerarse como un «caballo de Troya» potencial: la madre puede tener anticuerpos BVD positivos o negativos al momento de la prueba, BVDV negativo, pero aún puede tener un PI, ternero con antígeno positivo. T
- odos estos terneros deben ser probados al nacer para detectar BVDV y deben aislarse del rebaño hasta que nazca y se haga la prueba.
- Los animales que se extraviaron de la granja, o que entraron en contacto con animales que se extraviaron en la granja, deben mantenerse en cuarentena y analizarse según los animales comprados.
- El ganado que haya estado en un show o ventas debe ser puesto en cuarentena a su regreso.
- El equipo, los remolques y las instalaciones de manipulación que se comparten con otros rebaños de menor o desconocido estado de salud deben limpiarse y desinfectarse antes de su uso. Idealmente, este intercambio debe mantenerse al mínimo.
- Limite el acceso de la granja al personal esencial y proporcione overoles protectores.
- Los puntos de entrega y recogida deben estar lejos de los edificios de ganado.
- Donde sea posible, los conductores deben permanecer en sus cabinas.
- Use instalaciones de lavado y desinfección para visitantes y trabajadores.
Minimizando riesgos antes de la compra
Las compras de bajo riesgo son de rebaños que están acreditados por BVDFree England, o que tienen un estado de rebaño negativo a través de los esquemas BVDFree England y / o BVD Stamp It Out o equivalente. Además, una presa embarazada que es negativa para anticuerpos y virus, es poco probable que sea un animal troyano.
Las compras de alto riesgo son de rebaños donde se han divulgado varios animales PI en los últimos 12 meses, un rebaño que ha tenido un resultado no negativo en la evaluación anual a través de los esquemas BVDFree England o BVD Stamp It Out, o animales preñados sin prueba / historia.
¿Podemos permitirnos no erradicar la BVD?
El costo de BVD para la industria se estima entre hasta £ 61 millones por año. Si bien esta cifra es un poco sorprendente, puede ser difícil comprender la realidad y, en términos más familiares, se ha estimado que esto puede equivaler a £ 4,500 por año para el rebaño de carne de vacuno de 100 vacas, o £ 15,000 al año por el rebaño de ordeño de 130 vacas.
Una presentación de la Conferencia del Centro de Expertos en Brotes de Enfermedades Animales de 2019 mostró que el análisis económico de la introducción de un animal PI en un rebaño ingenuo generó un costo de £ 55 por vaca en el rebaño de carne y £ 35 por vaca en el rebaño lechero, con abortos de hasta 5.6% y pérdida de leche de 64.5L.
Sin embargo, en última instancia, los principales beneficios para erradicar la BVD deben verse como aquellos tangibles en la granja: existencias más saludables y ganancias más saludables. Está bien demostrado que, al erradicar los animales con IP de la granja, la salud del ganado joven debería mejorar. En los programas de erradicación11, los tratamientos de pantorrillas para la neumonía y las diarreas se redujeron a casi cero después de que se eliminaron todos los animales con IP. Este es un beneficio adicional en un momento en que las granjas y los veterinarios que prescriben están bajo un escrutinio cada vez mayor con respecto al uso de antibióticos. Los terneros que han estado enfermos con neumonía o diarrea nunca pueden alcanzar su máximo potencial, y los efectos se pueden sentir hasta que producen sus propios terneros y entran en su propio ciclo productivo.
Se agrega un estrés psicológico significativo al agricultor, al propietario o al personal de la granja donde existen múltiples problemas de salud. Es probable que una granja con BVD en circulación activa sufra una fertilidad deficiente, lo que irá de la mano con una baja productividad, una baja producción y flujo de caja, así como también es probable que tenga crías enfermas y moribundas. A su vez, esto requiere más mano de obra y puede agotar rápidamente las reservas físicas y mentales de la mayoría de nuestros clientes.
Vacunación
La vacunación (Tabla 1) ha estado disponible y se ha utilizado ampliamente en el Reino Unido durante más de 15 años. Hubo un tiempo en que los agricultores y los veterinarios pudieron haberlo percibido por igual como una cura, sin ningún control activo o búsqueda de PI.
Este método de control no puede verse como completo y los animales PI deben buscarse en un programa de erradicación. Además, el uso histórico de un IP como animal vacunador no puede considerarse una política de control eficaz y está desactualizado.
¿Cuándo vacunar? Una vez evaluados los riesgos, se recomienda la vacunación cuando sea posible una posible violación de la bioseguridad. La vacunación ofrece una protección rentable de la presa, eliminando así la producción de animales PI y la propagación de enfermedades dentro del rebaño. Se causaron daños considerables en Baja Sajonia, Alemania, donde el BVDV se reintrodujo en rebaños que se habían vuelto seronegativos después de la erradicación, en la medida en que algunas autoridades estatales ahora subsidian y ordenan la vacunación6.
Al igual que con todas las vacunas BVD, el objetivo es que todas las especies reproductoras hayan completado su ciclo primario 3 a 4 semanas antes del servicio, para garantizar la protección fetal completa, eliminando el riesgo de que la madre produzca un feto PI.
Al igual que con todos los protocolos de vacunación, el cumplimiento estricto de las recomendaciones de los fabricantes para el almacenamiento, el tiempo y el método de entrega es fundamental para una protección sólida (Figura 6).
Las fallas de la vacuna para detener la propagación de la enfermedad se deben a un momento incorrecto o al incumplimiento correcto del ciclo primario de dos vacunas. La introducción más reciente de un curso primario de una sola vez ofrece protección contra ambos tipos de BVD 1 y 2, al tiempo que tiene un programa de administración simple para que los agricultores se adhieran, ayudando al cumplimiento.
Tenga en cuenta que aunque el objetivo principal de la vacunación es detener la producción de futuros animales con IP en la granja, donde existe una infección activa, la vacunación de los terneros para proteger contra el BVD tipo 1 tiene como objetivo reducir el efecto inmunosupresor y reducir la eliminación del virus en esa población.
En resumen
Es claro ver desde Europa que los esquemas de erradicación de BVD pueden ser exitosos. Si bien BVDFree England y BVD Stamp It Out se han lanzado como iniciativas voluntarias, debe seguirse un requisito legal para que todas las explotaciones cumplan.
Es esencial que los veterinarios y los agricultores trabajen juntos para lograr el éxito aquí. Nada puede ser más gratificante que mejorar la salud general del rebaño y proporcionar un mercado transparente para el comercio de animales.
Referencias
- Bøtner A and Belsham GJ (2012). Virus survival in slurry: analysis of the stability of foot-and-mouth disease, classical swine fever, bovine viral diarrhoea and swine influenza viruses, Veterinary Microbiology 157(1-2): 41-49.
- Couchinho RMC. APHA trojan cows presentation.
- Niskanen R and Lindberg A (2003). Transmission of bovine viral diarrhoea virus by unhygienic vaccination procedures, ambient air, and from contaminated pens, The Veterinary Journal 165(2): 125-130.
- Drew T, David G and Steinbach F et al (2007). Occurrence of a second strain of BVDV-2 in the UK, Veterinary Record 160(23): 810.
- Booth R, MacGillivray F, Armstrong D and Brownlie J (2016). Control of bovine viral diarrhoea virus at the national level: a brief summary of European BVD control past, present and future, UK-Vet Livestock 21(6): 338-345.
- Metcalfe LVA (2019). An update on the status of BVD control and eradication in Europe, J Veter Sci Med 7(1): 4.
- BVD Free England (www.bvdfree.org.uk).
- Booth RE, Cranwell MP and Brownlie J (2013). Monitoring the bulk milk antibody response to BVD: the effects of vaccination and herd infection status, Veterinary Record 172(17): 449.
- Voges H, Horner GW, Rowe S and Wellenberg GJ (1998). Persistent bovine pestivirus infection localized in the testes of an immune-competent, non-viraemic bull, Veterinary Microbiology 61(3): 165-175.
- Waters A (2019). BVD eradication steps up a gear, Veterinary Record 185(3): 67.
- Booth RE and Brownlie J (2012). Establishing a pilot bovine viral diarrhoea virus eradication scheme in Somerset, Veterinary Record 170(3): 73.
Lecturas recomendadas
- Booth RE (2015). A Practical Guide to Diagnosing and Eradicating Bovine Viral Diarrhoea (BVD) Virus, MSD Animal Health.
- Brownlie J, Clarke MC, Howard CJ and Pocock DH (1987). Pathogenesis and epidemiology of bovine virus diarrhoea virus infection of cattle, Annales de Recherches Vétérinaires 18(2): 157-166.
- Brownlie J, Thompson I and Curwen A (2000). Bovine virus diarrhoea virus – strategic decisions for diagnosis and control, In Practice 22(4): 176-187.
- Byrne AW, Guelbenzu-Gonzalo M, Strain SAJ, McBride S, Graham J, Lahuerta-Marin A, Harwood R, Graham DA and McDowell S (2017). Assessment of concurrent infection with BVDV and Mycobacterium bovis: a herd level risk factor analysis from Northern Ireland, Preventive Veterinary Medicine 141: 38-47.
- Courtenay AE, Henderson RG, Cranwell MP and Sandvik T (2007). BVD virus type 2 infection and severe clinical disease in a dairy herd, Veterinary Record 160(20): 706-707.
- Gunn GJ, Stott AW and Humphry RW (2004). Modelling and costing BVD outbreaks in beef herds, The Veterinary Journal 167(2): 143-149.
- Price R and Priestley M (2016). BVD forum: joint approach needed to tackle disease, Farmers Weekly, https://bit.ly/2RWTxIz
- Van Campen H, Frölich K and Hofmann M (2001). Pestivirus infections. In Williams ES and Barker IK (eds), Infectious Diseases of Wild Mammals (3rd edn), Iowa State University Press, Ames: 232-244.

